
機械設備電腦確效作業與 21 CFR Part 11簡介
由ISPE所制訂的GAMP和GMP不一樣,它不屬於強制性的規範和標準,而是一個理論和實踐方法上的指南。因為它不屬於規範,ISPE也不屬於認證機構,所以在GAMP中也聲明:任何宣稱“已通過GAMP認證”或“已獲得GAMP批准”是不合適的。
但GAMP5所提出許多理論和概念還是非常科學和有道理的,所以雖然它不屬於法規,但卻是目前國際製藥行業進行電腦化系統驗證方法的主要參考依據, 同時也是醫藥自動化最重要的法規性指南。
一、流程
應首先建立一個概念,電腦系統的驗證不只局限於系統的使用過程,新系統的驗證應始於系統初期的定義和設計階段,終止於系統無使用價值階段。驗證生命週期(SVLC)應伴隨著系統發展的整個生命週期(SDLC)。
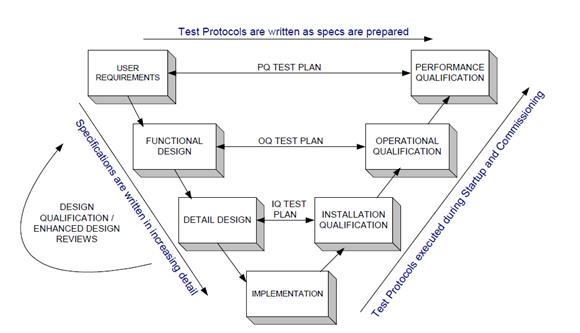
系統發展的生命週期可劃分為以下8 個階段:
1、 可行性研究
2、 工程計畫
3、 需求定義
4、 系統設計
5、 系統測試
6、 系統驗收及確認
7、 使用和維護
8、 系統引退
二、基礎架構
GAMP 5 對電腦化系統軟體的分類
第1類軟體:基礎結構軟體(Infrastructure Software )
第3類軟體:不可配置軟體 ( Non-Configured Products )
第4類軟體:可配置軟體 ( Configured Products )
第5類軟體:訂製應用軟體 (Custom Application)
電腦化系統硬體的分類
第1類硬體:標準硬體元件(Standard Hardware Components)(目前採用的大部分的都是這類硬體)
第2類硬體:定加工硬體元件(Custom Build Hardware Components)(這類硬體是為了滿足特殊需要而開發的,是對標準硬體件元件的補充)
三、驗證
系統驗收及驗證,當最終的電腦系統及相關的檔發至用戶,其被安裝在用戶環境中並評價其功能的正確性。
驗證(〝安裝驗證〞、〝運行驗證〞及〝性能驗證〞)是電腦系統付之實際使用之前的既完整又系統的測試行為,它直接影響到電腦系統的使用品質。也就是說,〝驗證〞是電腦系統品質保證的最後一個環節。儘管〝驗證〞的某些部分是在單元測試和組裝測試相同的條件下進行的,而且所用的資料相同,但〝驗證〞仍是必要的。
〝驗證〞一般由用戶執行。
驗證主要動作
1、 執行經核准的協議
2、 觀察執行結果
3、 記錄觀察意見
4、 撰寫執行報告
5、 核准報告,或依變更管制流程重新執行 (修改或核准)
四、21 CFR Part 11

元成機械可提供符合21 CFR Part 11文件
CFR:Code of Federal Regulations
21 CFR Part 11,即是美國聯邦法規第21章第11款,至於此一規範的主要宗旨,係在於針對文件內容中所涉及之電子記錄、電子簽章,制定出具體規定。
聯邦法規21章第11 款
電子記錄;電子簽名
分章A 一般規定
11.1適用範圍
11.2 履行
11.3 定義
分章B 電子記錄
11.10 封閉系統的控制
11.30 開放系統的控制
11.50 簽名的驗證
11.70 簽名/記錄連接
分章C 電子簽章
一般規定
電子簽章和控管
控管識別碼/密碼
元成機械設備可提供以上服務
Reference from GAMP5 and 21 CFR Part 11


